A pneumonía nosocomial é a infección nosocomial máis común e grave, da cal a pneumonía asociada á ventilación mecánica (NAV) representa o 40 %. A NAV causada por patóxenos refractarios segue a ser un problema clínico complexo. Durante anos, as guías recomendaron unha serie de intervencións (como a sedación dirixida e a elevación da cabeza) para previr a NAV, pero a NAV prodúcese en ata un 40 % dos pacientes con intubación traqueal, o que provoca estancias hospitalarias máis longas, un maior uso de antibióticos e a morte. A xente sempre busca medidas preventivas máis eficaces.
A pneumonía asociada á ventilación mecánica (NAVM) é unha nova forma de pneumonía que se desenvolve 48 horas despois da intubación traqueal e é a infección nosocomial máis común e mortal na unidade de coidados intensivos (UCI). As directrices da Sociedade Americana de Enfermidades Infecciosas de 2016 distinguiron a NAVM da definición de pneumonía adquirida no hospital (NAPM) (a NAPM só se refire á pneumonía que se produce despois da hospitalización sen tubo traqueal e non está relacionada coa ventilación mecánica; a NAVM é a pneumonía despois da intubación traqueal e a ventilación mecánica), e a Sociedade Europea e China cren que a NAVM segue sendo un tipo especial de NAPM [1-3].
En pacientes que reciben ventilación mecánica, a incidencia de VAP oscila entre o 9 % e o 27 %, a taxa de mortalidade estímase no 13 % e pode levar a un aumento do uso sistémico de antibióticos, ventilación mecánica prolongada, estancia prolongada na UCI e aumento dos custos [4-6]. A HAP/VAP en pacientes non inmunodeficientes adoita estar causada por unha infección bacteriana, e a distribución dos patóxenos comúns e as súas características de resistencia varían segundo a rexión, a clase hospitalaria, a poboación de pacientes e a exposición a antibióticos, e cambian co tempo. Pseudomonas aeruginosa dominou os patóxenos relacionados con VAP en Europa e América, mentres que se illaron máis Acinetobacter baumannii en hospitais terciarios da China. Entre un terzo e a metade de todas as mortes relacionadas con VAP son causadas directamente pola infección, sendo maior a taxa de mortalidade dos casos causados por Pseudomonas aeruginosa e acinetobacter [7,8].
Debido á forte heteroxeneidade da VAP, a especificidade diagnóstica das súas manifestacións clínicas, probas de imaxe e de laboratorio é baixa, e o rango de diagnóstico diferencial é amplo, o que dificulta o diagnóstico da VAP a tempo. Ao mesmo tempo, a resistencia bacteriana supón un serio desafío para o tratamento da VAP. Estímase que o risco de desenvolver VAP é do 3 %/día durante os primeiros 5 días de uso da ventilación mecánica, do 2 %/día entre 5 e 10 días e do 1 %/día durante o resto do tempo. A incidencia máxima xeralmente ocorre despois de 7 días de ventilación, polo que hai unha xanela na que se pode previr a infección precozmente [9,10]. Moitos estudos analizaron a prevención da VAP, pero a pesar de décadas de investigación e intentos para previr a VAP (como evitar a intubación, previr a reintubación, reducir a sedación, elevar a cabeceira da cama de 30° a 45° e coidado bucal), a incidencia non parece ter diminuído e a carga médica asociada segue a ser moi alta.
Os antibióticos inhalados empregáronse para tratar infeccións crónicas das vías respiratorias desde a década de 1940. Debido a que poden maximizar a subministración de fármacos ao lugar obxectivo da infección (é dicir, as vías respiratorias) e reducir os efectos secundarios sistémicos, demostraron un bo valor de aplicación nunha variedade de enfermidades. Os antibióticos inhalados están agora aprobados pola Administración de Alimentos e Medicamentos dos Estados Unidos (FDA) e a Axencia Europea de Medicamentos (EMA) para o seu uso na fibrose quística. Os antibióticos inhalados poden reducir significativamente a carga bacteriana e a frecuencia das exacerbacións na bronquiectasia sen aumentar os eventos adversos globais, e as directrices actuais recoñecéronos como tratamento de primeira liña para pacientes con infección por pseudomonas aeruginosa e exacerbacións frecuentes; Os antibióticos inhalados durante o período perioperatorio do transplante de pulmón tamén se poden usar como fármacos adxuvantes ou profilácticos [11,12]. Pero nas directrices VAP dos Estados Unidos de 2016, os expertos carecían de confianza na eficacia dos antibióticos inhalados adxuvantes debido á falta de grandes ensaios controlados aleatorios. O ensaio de fase 3 (INHALE) publicado en 2020 tampouco obtivo resultados positivos (antibióticos intravenosos asistidos por amikacina inhalada para infección bacteriana gramnegativa causada por pacientes con VAP, un ensaio de eficacia de fase 3, dobre cego, aleatorizado e controlado con placebo, cun total de 807 pacientes, medicación sistémica + inhalación asistida de amikacina durante 10 días).
Neste contexto, un equipo dirixido por investigadores do Centro Hospitalario Universitario Rexional de Tours (CHRU) en Francia adoptou unha estratexia de investigación diferente e levou a cabo un ensaio de eficacia controlado, aleatorio, dobre cego e multicéntrico iniciado por un investigador (AMIKINHAL). Comparouse a amikacina inhalada ou o placebo para a prevención da VAP en 19 UCI en Francia [13].
Un total de 847 pacientes adultos con ventilación mecánica invasiva entre 72 e 96 horas foron asignados aleatoriamente 1:1 a inhalación de amikacina (N = 417,20 mg/kg de peso corporal ideal, QD) ou inhalación de placebo (N = 430, equivalente a cloruro de sodio ao 0,9%) durante 3 días. O criterio de valoración principal foi o primeiro episodio de ventilación mecánica invasiva (NAV) desde o inicio da asignación aleatoria ata o día 28.
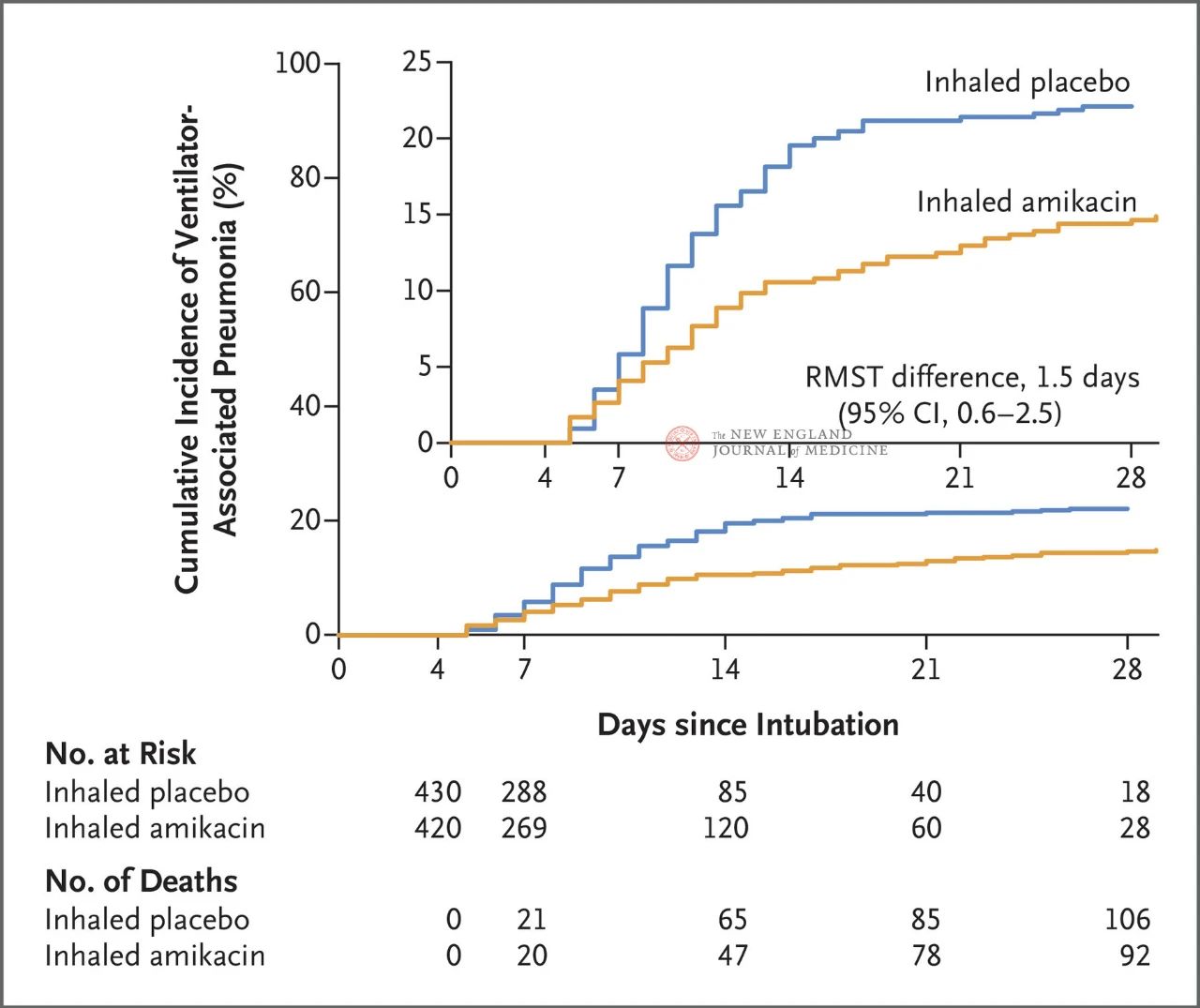
Os resultados do ensaio mostraron que aos 28 días, 62 pacientes (15 %) do grupo de amikacina desenvolveran NAV e 95 pacientes (22 %) do grupo placebo desenvolveran NAV (a diferenza media limitada de supervivencia para a NAV foi de 1,5 días; IC do 95 %, 0,6~2,5; P=0,004).
En termos de seguridade, sete pacientes (1,7 %) no grupo de amikacina e catro pacientes (0,9 %) no grupo placebo experimentaron eventos adversos graves relacionados co ensaio. Entre os que non tiveron lesión renal aguda na aleatorización, 11 pacientes (4 %) no grupo de amikacina e 24 pacientes (8 %) no grupo placebo tiveron lesión renal aguda no día 28 (HR, 0,47; IC do 95 %, 0,23~0,96).
O ensaio clínico tivo tres aspectos destacados. En primeiro lugar, en termos do deseño do estudo, o ensaio AMIKINHAL baséase no ensaio IASIS (un ensaio de fase 2 paralelo, aleatorizado, dobre cego, controlado con placebo, no que participaron 143 pacientes). Para avaliar a seguridade e a eficacia da inhalación de amikacina-fosfomicina para o tratamento sistémico da infección bacteriana gramnegativa causada por VAP) e no ensaio INHALE, as leccións aprendidas, que se centran na prevención da VAP, obtiveron resultados relativamente bos. Debido ás características de alta mortalidade e longa estancia hospitalaria en pacientes con ventilación mecánica e VAP, se a inhalación de amikacina pode lograr resultados significativamente diferentes na redución da morte e a estancia hospitalaria nestes pacientes, será máis valiosa para a práctica clínica. Non obstante, dada a heteroxeneidade do tratamento e a atención tardía en cada paciente e cada centro, hai unha serie de factores de confusión que poden interferir co estudo, polo que tamén pode ser difícil obter un resultado positivo atribuíble aos antibióticos inhalados. Polo tanto, un estudo clínico exitoso require non só un excelente deseño de estudo, senón tamén a selección de criterios de valoración primarios axeitados.
En segundo lugar, aínda que os antibióticos aminoglicósidos non se recomendan como fármaco único en varias directrices de VAP, os antibióticos aminoglicósidos poden cubrir patóxenos comúns en pacientes con VAP (incluíndo Pseudomonas aeruginosa, Acinetobacter, etc.), e debido á súa limitada absorción nas células epiteliais pulmonares, alta concentración no lugar da infección e baixa toxicidade sistémica. Os antibióticos aminoglicósidos son amplamente preferidos entre os antibióticos inhalados. Este artigo é consistente coa estimación exhaustiva do tamaño do efecto da administración intratraqueal de gentamicina en pequenas mostras publicada anteriormente, o que demostra conxuntamente o efecto dos antibióticos aminoglicósidos inhalados na prevención da VAP. Tamén cómpre sinalar que a maioría dos controis placebo seleccionados nos ensaios relacionados cos antibióticos inhalados son solución salina normal. Non obstante, considerando que a inhalación atomizada de solución salina normal en si mesma pode desempeñar un certo papel na dilución do esputo e na axuda expectorante, a solución salina normal pode causar certa interferencia na análise dos resultados do estudo, o que debe considerarse exhaustivamente no estudo.
Ademais, a adaptación local da medicación para HAP/VAP é importante, do mesmo xeito que a profilaxe con antibióticos. Ao mesmo tempo, independentemente da duración do tempo de intubación, a ecoloxía da UCI local é o factor de risco máis importante para a infección por bacterias multirresistentes. Polo tanto, o tratamento empírico debe referirse aos datos microbiolóxicos dos hospitais locais na medida do posible, e non pode referirse cegamente ás directrices ou á experiencia dos hospitais terciarios. Ao mesmo tempo, os pacientes en estado crítico que requiren ventilación mecánica adoitan presentar enfermidades multisistémicas e, baixo a acción combinada de múltiples factores, como o estado de estrés, tamén pode haber un fenómeno de comunicación cruzada dos microbios intestinais cos pulmóns. A alta heteroxeneidade das enfermidades causadas pola superposición interna e externa tamén determina que a promoción clínica a grande escala de cada nova intervención aínda está lonxe.
Data de publicación: 02-12-2023